|
Oksidasi Swern
Oksidasi Swern, dinamai dari Daniel Swern, adalah suatu reaksi kimia di mana alkohol primer atau sekunder teroksidasi menjadi suatu aldehida atau keton menggunakan oksalil klorida, dimetil sulfoksida (DMSO) dan basa organik, seperti trietilamina.[1][2][3] Reaksi ini dikenal dengan karakternya yang ringan dan toleransi yang luas pada gugus fungsional.[4][5][6][7]  Produk samping reaksi ini adalah dimetil sulfida (Me2S), karbon monoksida (CO), karbon dioksida (CO2) dan — ketika trietilamina digunakan sebagai basa — trietilamonium klorida (Et3NHCl). Dua dari produk samping tersebut, dimetil sulfida dan karbon monoksida, adalah senyawa volatil yang sangat beracun, sehingga reaksi dan pengerjaan perlu dilakukan dalam lemari asam.[8][9][10] MekanismeTahapan pertama pada reaksi oksidasi Swern adalah reaksi dimetil sulfoksida (DMSO) pada suhu rendah, 1a, secara formal sebagai kontributor dalam resonansi 1b, dengan oksalil klorida, 2. Zat antara pertama, 3, secara cepat terurai menghasilkan CO2 dan CO dan memproduksi kloro(dimetil)sulfonium klorida, 4. 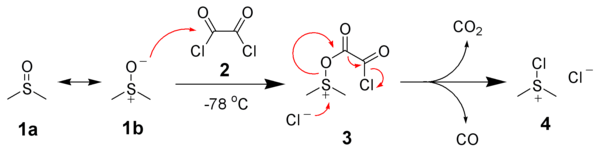 Setelah penambahan alkohol 5, kloro(dimetil)sulfonium klorida 4 bereaksi dengan alkohol untuk memberi ion intermediet penting alkoksisulfonium, 6. Penambahan minimal 2 ekivalen basa - biasanya trietilamina - akan mendeprotonasi ion alkoksisulfonium untuk menghasilkan sulfur ilida 7. Dalam keadaan transisi cincin beranggota-5, sulfur ilida 7 terurai untuk menghasilkan dimetil sulfida dan keton yang diinginkan (atau aldehida) 8. 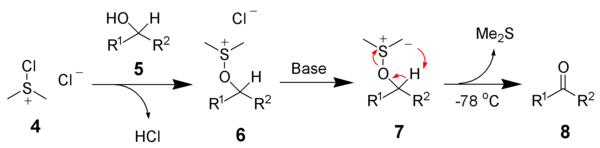 VariasiBila menggunakan oksalil klorida sebagai agen dehidrasi, reaksi harus dijaga lebih dingin dari −60 °C untuk menghindari reaksi samping. Dengan sianurat klorida[11] atau anhidrida trifluoroasetat dan bukan oksalil klorida, reaksi dapat dihangatkan sampai −30 °C tanpa reaksi samping. Metode lain untuk mengaktifkan DMSO untuk memulai pembentukan intermediet kunci 6 adalah penggunaan karbodiimida (oksidasi Pfitzner–Moffatt) dan kompleks piridina-sulfur trioksida (oksidasi Parikh-Doering). Zat antara 4 juga dapat dibuat dari dimetil sulfida dan N-klorosuksinimida (oksidasi Corey-Kim). Dalam beberapa kasus, penggunaan trietilamina sebagai basa dapat menyebabkan epimerisasi di bagian karbon pada karbonil yang baru dibentuk. Menggunakan basa diisopropiletilamina (iPr2NEt, basa Hünig) yang lebih meruah dapat mengurangi reaksi samping tersebut. PertimbanganDimetil sulfida, hasil samping oksidasi Swern, adalah salah satu senyawa dengan bau yang paling busuk yang dikenal dalam kimia organik. Kelenjar penciuman manusia dapat mendeteksi senyawa ini dalam konsentrasi serendah 0.02-0.1 bagian per juta.[12] Penanganan sederhana untuk masalah ini adalah untuk membilas gelas kimia yang digunakan dengan pemutih (biasanya mengandung natrium hipoklorit), yang akan mengoksidasi dimetil sulfida, yang dapat menghilangkan bau tersebut. Kondisi reaksi memungkinkan oksidasi senyawa yang sensitif terhadap asam, yang mungkin membusuk di bawah kondisi asam pada metode tradisional seperti oksidasi Jones. Misalnya, dalam sintesis Thompson & Heathcock pada seskuiterpena isovelleral,[13] tahapan akhir menggunakan protokol Swern, untuk menghindari penataan pada bagian siklopropanametanol yang sensitif terhadap asam.  Lihat pulaReferensi
Pranala luar |
||||||||||||||