|
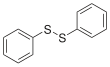
Disulfuro de difenilo
El disulfuro de difenilo es el compuesto químico de fórmula (C6H5S)2. Este material cristalino incoloro a menudo se abrevia como Ph2S2. Es uno de los disulfuros orgánicos que se encuentran más comúnmente en la síntesis orgánica. Una contaminación menor por tiofenol es responsable del olor desagradable asociado con este compuesto. Preparación y estructuraEl disulfuro de difenilo suele prepararse mediante la oxidación de tiofenol :
También se puede utilizar peróxido de hidrógeno como oxidante. El Ph 2 S 2 rara vez se prepara en el laboratorio porque es económico y el precursor tiene un olor desagradable. Como la mayoría de los disulfuros orgánicos, el núcleo C – S – S – C de Ph 2 S 2 no es plano con un ángulo diédrico que se acerca a los 85 °. [2]  ReaccionesEl Ph2S2 se utiliza principalmente en síntesis orgánica como fuente del sustituyente PhS.[3] Una reacción típica implica la formación de compuestos carbonílicos sustituidos por PhS a través del enolato:
ReducciónEl Ph2S2 sufre una reducción, una reacción característica de los disulfuros:
También se pueden utilizar como reductores reactivos de hidruro tales como borohidruro de sodio y superhidruro. Las sales PhSM son fuentes del potente nucleófilo PhS−. La mayoría de los haluros de alquilo, RX (X = haluro), los convierten en tioéteres con la fórmula general RSPH. De manera análoga, la protonación de MSPH da tiofenol:
HalogenaciónPh2S2 reacciona con cloro para dar cloruro de fenilsulfenilo PhSCl (escisión por disulfuro de Zincke). Esta especie suele generarse y utilizarse in situ. Con difluoruro de xenón, el Ph2S2 reacciona para dar pentafluoruro de fenilazufre. [4] Catalizador para la fotoisomerización de alquenos.El Ph2S2 cataliza la isomerización cis - trans de alquenos bajo irradiación UV. La oxidación del Ph2S2 con acetato de plomo (IV) (Pb(OAc)4) en metanol produce el éster de sulfinito PhS(O)OMe.[5] Referencias
Enlaces externos
|
|||||||||||||||||||||||||||||||||||||||||||||