|
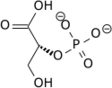
Acide phosphoénolpyruvique
L’acide phosphoénolpyruvique — ou phosphoénolpyruvate sous forme déprotonée, abrégée en PEP — est un composé organique important en biochimie, en raison notamment de son groupe phosphate à haut potentiel de transfert (ΔG°' = −61,9 kJ mol−1, valeur la plus élevée trouvée chez les êtres vivants). Il intervient par conséquent comme métabolite de la glycolyse en relation avec la chaîne respiratoire, fournissant l'énergie nécessaire à la phosphorylation d'une molécule d'ADP en ATP. Il intervient également comme accepteur de CO2 hydraté (HCO3-) chez les plantes au métabolisme C4 ou CAM, pour former l'oxaloacétate, dans une réaction catalysée par la phosphoénolpyruvate carboxylase. Rôle dans la glycolyse
BiosynthèseLe 2-phospho-D-glycérate (2PG) produit au cours de la glycolyse est déshydraté par une lyase, l’énolase (ou phosphopyruvate hydratase), pour former le phosphoénolpyruvate (PEP). Un cation Mg2+ est requis comme « catalyseur » de la réaction de déshydratation, tandis qu'un second Mg2+ intervient avec un rôle « conformationnel » en coordination avec le groupe carboxyle du 2PG. DégradationLe groupe phosphate à haut potentiel de transfert (ΔG°' = −61,9 kJ mol−1) du PEP permet la phosphorylation d'une molécule d'ADP en ATP par la pyruvate kinase. Un cation Mg2+ est nécessaire à cette réaction comme cofacteur. Notes et références
Voir aussi |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||