|
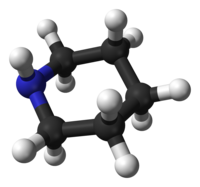
Piperidin
A piperidin (vagy a Hantzsch–Widman-nevezéktan szerint azinán) szerves vegyület, képlete (CH2)5NH. Heterociklusos amin, melynek hattagú gyűrűjében öt metilén egység és egy nitrogénatom található. Színtelen, füstölgő folyadék, szaga ammóniás, a borsra emlékeztető;[4] neve a Piper nemzetségnévből származik, mely a bors latin neve.[5] A piperidint szerves kémiai szintézisekben – beleértve a gyógyszergyártást is – széles körben használják mint reagenst és szerkezeti alapegységet. ElőállításaIparilag a piperidint a piridin hidrogénezésével állítják elő, melyet többnyire molibdén-diszulfid katalizátor felett végeznek:[6]
A piridin etanolban nátriummal is piperidinné redukálható.[7] A piperidin és származékai természetes előfordulásaMagát a piperidint borsból,[8] Psilocaulon absimile N.E.Br (Aizoaceae)[9] és a Petrosimonia monandra növényből nyerték.[10] A piperidin szerkezeti egység számos természetes alkaloidban megtalálható. Ezek közé tartozik a piperin, amely a feketebors csípős ízét okozza. A vegyület neve is innen származik. További példák a tűzhangyák toxinja, a szolenopszin,[11] a nikotin-analóg anabazin, mely a dohányfában (Nicotiana glauca) található meg, az indián dohányban levő lobelin, és a koniin, a foltos bürök mérgező alkaloidja, mely Szókratész halálát okozta.[12] KonformációjaA piperidin esetén – a ciklohexánhoz hasonlóan – a szék konformáció az előnyösebb, azonban a ciklohexántól eltérően két megkülönböztethető szék konformáció létezik: az egyikben az N–H kötés axiális helyzetű, míg a másikban ekvatoriális pozíciót foglal el. Az 1950–70-es évek számos vitáját követően az ekvatoriális konformáció bizonyult stabilabbnak, az energiakülönbség gázfázisban 0,72 kcal/mol.[13] Nem poláris oldószerekben 0,2–0,6 kcal/mol közötti értéket becsülnek, de poláris oldószerekben előfordulhat, hogy az axiális konformáció a stabilabb.[14] A két konformer a nitrogéninverzió révén gyorsan egymásba alakul, a folyamat aktiválási szabadenergiáját 6,1 kcal/mol értékűnek becsülik, ami jelentősen kevesebb a gyűrűinverzió 10,4 kcal/mol értékénél.[15] Az N-metilpiperidin esetén az ekvatoriális konformáció 3,16 kcal/mol-lal stabilabb,[13] ami jóval magasabb a metilciklohexán 1,74 kcal/mol értékénél.
ReakcióiA piperidin széleskörűen alkalmazott szekunder amin. Elterjedten használják ketonokból enaminok előállítására.[16] A piperidinből nyert enaminok felhasználhatók a Stork enamin alkilezési reakcióban.[17] A piperidin kalcium-hipoklorittal a C5H10NCl klóraminná alakítható. Az így kapott klóramin dehidrohalogénezés során gyűrűs iminné alakul.[18] NMR kémiai eltolódások13C NMR = (CDCl3, ppm) 47,5, 27,2, 25,2 FelhasználásaA piperidint oldószerként és bázisként használják. Ugyanez mondható el egyes származékaira is: az N-formilpiperidin poláris aprotikus oldószer, mely a szénhidrogéneket jobban oldja, mint más amid oldószerek, míg a 2,2,6,6-tetrametilpiperidin sztérikusan zsúfolt bázis, mely alacsony nukleofilitása és szerves oldószerekben való jó oldhatósága miatt használható előnyösen. A piperidin jelentős ipari alkalmazása a dipiperidinil ditiurám tetraszulfid előállítása során történő felhasználása, ez a vegyület a gumi vulkanizálásakor gyorsítóként használatos.[6] Ezeken kívül a piperidin és származékai gyakran használt építőegységek a gyógyszervegyületek és finomvegyszerek szintézise során. A piperidin egység megtalálható például az alábbi gyógyszerekben: paroxetin, riszperidon, metilfenidát, raloxifen, minoxidil, tioridazin, haloperidol, droperidol, mezoridazin, meperidin, melperon, továbbá a Ditran-B (JB-329), N-metil-3-piperidil-benzilát (JB-336) és számos más pszichokémiai vegyületben. A piperidint lebontási kémiai reakciókban – például egyes módosított nukleotidok hasításával a DNS-szekvenálása során – is rendszeresen használják. A szilárdfázisú peptidszintézis során az Fmoc-aminosavak védőcsoportjának eltávolításakor a piperidint gyakran használják mint bázist. FordításEz a szócikk részben vagy egészben a Piperidine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként. Hivatkozások
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||