|
Рідина
Рідина́ — один з основних агрегатних станів речовини нарівні з газом та твердим тілом. Від газу рідина відрізняється тим, що зберігає свій об'єм, а від твердого тіла тим, що не зберігає форми. Рух рідин та тіл в рідинах вивчає розділ фізики гідродинаміка, будову та фізичні властивості рідин — фізика рідин, складова частина молекулярної фізики. Загальна характеристикаРідина — конденсований агрегатний стан речовини, проміжний між твердим та газоподібним. Фізичне тіло, якому притаманні:
Збереження об'єму, густина, показник заломлення, теплота плавлення, в'язкість — властивості, які зближують рідини з твердими тілами, а незбереження форми — з газами. Для рідин характерний ближній порядок розташування молекул (відносна впорядкованість у розташуванні молекул найближчого оточення довільної молекули, подібна до порядку в кристалічних тілах, але на відстані кількох атомних діаметрів ця впорядкованість порушується). Взаємодія між молекулами рідини здійснюється Ван дер Ваальсовими і водневими зв'язками. Рідини, крім розсолів та зріджених металів, — погані провідники електричного струму.  Плинність рідин пов'язана з періодичним «перестрибуванням» їхніх молекул з одного рівноважного положення в інше. Більшу частину часу окрема молекула рідини перебуває в тимчасовій асоціації з сусідніми молекулами (ближня впорядкованість), де вона здійснює теплові коливання. Інколи рідиною в широкому розумінні слова називають і газ, при цьому рідину у вузькому змісті слова, яка задовольняє попереднім двом умовам, називають крапельною рідиною. У газів і крапельних рідин плинність проявляється вже при мінімальних напруженнях, тоді як у пластичних твердих тіл — лише при великих напруженнях, що перевищують границю текучості. Форма, яку приймає рідина, визначається формою ємності, в якій вона перебуває. Частинки рідини (зазвичай молекули або групи молекул) можуть вільно переміщуватися по всьому її об'єму, але сила взаємного притягання не дозволяє частинкам залишати цей об'єм. Об'єм рідини залежить від температури і тиску і є постійним за даних умов. Якщо об'єм рідини менший за об'єм ємності, в якій вона міститься, то можна спостерігати поверхню рідини. Поверхня має якості еластичної мембрани з поверхневим натягом, що дозволяє формуватися краплям та бульбашкам. Ще одним наслідком дії поверхневого натягу є капілярність. Зазвичай рідини не піддаються стисканню, наприклад, щоб помітно стиснути воду, необхідний тиск порядку гігапаскаля. Рідини в гравітаційному полі створюють тиск, як на стінки і дно ємності, так і на будь-які тіла всередині самої рідини. Цей тиск за законом Паскаля діє у всіх напрямках і зростає з глибиною. Якщо рідина перебуває в стані спокою в однорідному гравітаційному полі, тиск на будь-яку точку визначається барометричною формулою: де:
Згідно з цією формулою тиск на поверхні дорівнює нулю, тобто вважається, що посудина досить широка, й поверхневий натяг можна не враховувати. Зазвичай рідини розширюються при нагріванні та стискаються при охолоджуванні. Вода між 0 та 4 °C становить один з небагатьох винятків. В цьому діапазоні температур вода при зниженні температури збільшується в об'ємі. Рідина за температури кипіння перетворюється на газ, а за температури замерзання — на тверду речовину. Але навіть за температури, нижчій за температуру кипіння, рідина випаровується. Цей процес триває доти, доки не буде досягнуто рівноваги парціального тиску пари рідини та тиску на поверхні рідини. Саме через це жодна рідина не може існувати тривалий час у вакуумі. Всі рідини можна розділити на чисті рідини, що складаються з молекул однієї речовини, й суміші, які складаються з молекул різного сорту. Різні рідкі компоненти суміші можна розділити за допомогою фракційної дистиляції. Не всі рідини утворюють однорідну суміш, якщо помістити їх в одну посудину. Часто рідини не змішуються, утворюючи поверхню між собою. В полі тяжіння одна рідина може плавати на поверхні іншої. Здебільшого рідини — ізотропні речовини. Виняток складають рідкі кристали, які можна віднести до рідин з огляду на властивість перетікати й займати об'єм посудини, але в яких зберігаються властиві кристалічним тілам анізотропні властивості. Мікроскопічна будоваКласифікація рідинСтруктура та фізичні властивості рідини залежать від хімічної індивідуальності складових їх частинок та від характеру і величини взаємодії між ними. Можна виділити кілька груп рідин в порядку зростання складності.
Рідини перших двох груп (іноді трьох) зазвичай називають простими. Прості рідини вивчені краще від інших, з непростих рідин добре вивчена вода. У цю класифікацію не входять квантові рідини і рідкі кристали, які є особливими випадками і повинні розглядатися окремо. У рідині молекули здебільшого зберігають свою цілісність, хоча чимало рідин є розчинниками, в яких молекули до певної міри дисоціюють. При дисоціації в рідинах утворюються позитивно й негативно заряджені йони. Такі рідини проводять електричний струм (див. Електроліти). З мікроскопічної точки зору рідини відрізняються від твердих тіл відсутністю далекого порядку, а від газів — ближнім порядком. Це означає, що атоми й молекули рідин здебільшого перебувають щодо своїх сусідів у тих же положеннях, що й у твердому стані, однак цей порядок зберігається для наступного шару сусідів гірше, а надалі зовсім зникає. Ближній порядок у рідинах характеризують радіальною кореляційною функцією. Рух молекул у рідинахМолекули рідин здебільшого коливаються навколо тимчасового положення рівноваги, яке утворюється завдяки взаємодії з іншими молекулами. Для рідин потенціальна енергія взаємодії молекули з сусідами більша, ніж кінетична енергія теплового руху. Однак рідини характеризуються також високим коефіцієнтом самодифузії — з часом кожна молекула віддаляється від свого початкового положення. Середній квадрат зміщення від початкового положення молекули пропорційний часу. Структура рідин: близький порядок, радіальна функція розподілуЗавдяки взаємодії молекули в рідині розташовані не зовсім хаотично. Для характеристики взаємного положення молекул використовується поняття радіальної функції розподілу, яка пропорційна ймовірністі того, що на певній віддалі від якоїсь довільно-вибраної молекули, перебуватиме інша молекула. Для ідеального газу радіальна функція розподілу не залежить від віддалі і всюди дорівнює одиниці — рух молекул газу нескорельований, ймовірність знайти іншу молекулу на певній віддалі однакова. Для кристалу така функція розподілу складається із виразних максимумів, висота яких практично не зменшується з віддаллю. Говорять, що в кристалах зберігається далекий порядок. В рідинах радіальна функція розподілу має кілька максимумів, висота яких зменшується з віддаллю і через кілька середніх міжмолекулярних віддалей стає рівною одиниці. Говорять, що в рідинах зберігається ближній порядок, і не зберігається дальній порядок. Таким чином, рідини відносяться до конденсованих невпорядкованих систем. Експериментально радіальну функцію розподілу можна одержати, проаналізувавши дані експериментів із розсіяння рентгенівських променів чи нейтронів. Мала стисливість рідин пояснюється значним зростанням сил відштовхування між частинками рідини при незначному наближенні одної частинки до другої. Густина і питома вага рідиниГустина рідини — маса, її одиниці об'єму: де М — маса рідини в об'ємі W. Густина води за 4 °C ρ=1000 кг/м³. Якщо рідина неоднорідна, то ця формула визначає лише середню густину рідини. Для визначення густини в заданій точці слід скористатися формулою На практиці про масу рідини судять за її вагою. Вага рідини, що приходиться на одиницю об'єму, називається питомою вагою: де G — вага рідини в об'ємі W. Питома вага води при 4 °C γ = 9810 Н/м³ (1000 кгс/м³). Для неоднорідної рідини, щоб визначити питому вагу у точці, слід користуватись формулою: де ΔG — вага рідини в об'ємі ΔW. Густина та питома вага пов'язані між собою відомим співвідношенням де g — прискорення вільного падіння. Відносною питомою вагою рідини (чи відносною вагою) δ називається відношення питомої ваги даної рідини до питомої ваги води за 4°С: Ця величина є безрозмірнісною. Зміна об'єму (густини) рідиниЗміна об'єму рідини може відбуватись або в результаті зміни тиску (ця властивість має назву «стисливість»), або в результаті зміни температури (теплове розширення/стиснення). Стисливість рідинВсі реальні рідини у тій чи іншій мірі стискаються, тобто під дією зовнішнього тиску зменшують свій об'єм. Стисливість — це здатність рідини змінювати свій об'єм при зміні тиску. Стисливість рідини визначається рівнянням стану і, як правило, мала за величиною. Мала стисливість рідини обумовлена тим, що рідина характеризується сильною молекулярною взаємодією, а зміни величин тиску в технічних процесах порівняно невеликі. Враховуючи відносну малість тисків, що зустрічаються в реаліях допускають, що рідина стискається за законом Гука (по лінійній залежності). Мірою стисливості рідин служить коефіцієнт об'ємного стиснення рідини βS, що являє собою відносне зменшення об'єму V при підвищенні тиску p на одиницю: Знак «мінус» у формулі означає, що при збільшенні тиску об'єм зменшується. Якщо вважати, що одиницею тиску є Паскаль, то коефіцієнт об'ємного стиску буде вимірюватись у Па−1 (м²/Н). Пружність — це здатність рідини відновлювати свій об'єм після припинення дії зовнішніх силових впливів. Для якісної характеристики пружних властивостей використовують поняття модуля об'ємної пружності К, який, по суті, є оберненою величиною до коефіцієнта стисливості, тобто К=1/βS. Наприклад, для води βS=0,51·10−9 Па−1, що вказує на досить малу стисливість води. Гіпотетичну рідину, для якої βS=0, називають нестисливою. Теплове розширення рідинОскільки габаритні розміри рідин визначаються розмірами посудини, тому теплове розширення для рідин розглядається лише в об'ємному плані: де:
Коефіцієнт теплового розширення вказує на скільки зміниться початковий об'єм 1 м³ рідини при зростанні температури на 1 K або 1 °C). Коефіцієнт теплового розширення води при 20 °C становить αV = 2,07·10−4°C−1. В'язкість рідиниРідини характеризуються в'язкістю. Вона визначається як здатність чинити опір переміщенню однієї з частини рідини відносно іншої, тобто як внутрішнє тертя. Коли сусідні шари рідини рухаються один відносно одного, неминуче відбувається зіткнення молекул додатково до того, яке обумовлене тепловим рухом. Виникають сили, що загальмовують впорядкований рух. При цьому кінетична енергія упорядкованого руху переходить в теплову — енергію хаотичного руху молекул. У залежності від моделі в'язкості, яка покладена в основу розгляду в'язких характеристик рідин, вони поділяються на ньютонівські рідини (класична модель) і неньютонівські рідини. Текучість рідиниТекучість рідини — здатність частинок рідини сприймати в стані рівноваги найменші дотичні напруги (у зв'язку з чим даний об'єм рідини, що перебуває в стані спокою, завжди набуває форми посудини, в якій вона знаходиться). Характеризується коефіцієнтом текучості. Коефіцієнт текучості рідини обернений її динамічному коефіцієнту в'язкості. Син. — плинність рідини. Поняття про ідеальну рідинуУ багатьох випадках з достатньою для практики точністю у гідравліці можна знехтувати стисливістю рідини та опором розтягуванню і розглядати рідину як абсолютно нестисливу з відсутністю опору розтягуванню. У гідрогазодинаміці зустрічається низка задач, коли можна знехтувати і в'язкістю, приймаючи, що дотичні напруження відсутні так, як це спостерігається у рідині, що перебуває у стані спокою. Описана гіпотетична рідина з перерахованими властивостями, а саме:
називається ідеальною рідиною. Поняття «ідеальна рідина» вперше було введено Л.Ейлером. Така рідина є граничною абстрактною моделлю і лише наближено відображає об'єктивно існуючі властивості реальних рідин. Ця модель дає змогу з достатньою точністю розв'язувати багато дуже важливих питань гідрогазодинаміки і сприяє спрощенню складних задач. Поверхневий натяг, змочуваність і капілярні явищаПоверхневий натягРідина здатна утворювати вільну поверхню. Така поверхня є поверхнею розділу фаз даної речовини: по один бік знаходиться рідка фаза, по інший — газоподібна (пара), і, можливо, інші гази, наприклад, повітря. Поверхневий натяг — фізичне явище, суть якого в прагненні рідини скоротити площу своєї поверхні за незмінного об'єму. Своєю появою сили поверхневого натягу завдячують поверхневій енергії. Поверхневий натяг може бути пояснений притяганням між молекулами рідини. Він виникає як у випадку поверхні розділу між рідиною й газом, так і у випадку поверхні розділу двох різних рідин. Поверхнева енергія пропорційна площі поверхні поділу двох фаз S:
Коефіцієнт пропорційності σ, називають коефіцієнтом поверхневого натягу. Його значення залежить від природи дотичних середовищ. Цей коефіцієнт можна подати у вигляді де F — сила поверхневого натягу;
 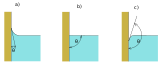  Поверхневий натяг рідини чутливий до її чистоти, складу і температури. Речовини, здатні значною мірою знизити сили поверхневого натягу, називаються поверхнево-активними речовинами (ПАР). При підвищенні температури величина сил поверхневого натягу зменшується, а в критичній точці кипіння рідини прямує до нуля. На межі поділу вода — повітря за t=20°С коефіцієнт поверхневого натягу σ=0,073 Дж/м², а для межі поділу ртуть — повітря коефіцієнт σ=0,48 Дж/м². Змочуваність рідинНа поверхні поділу трьох фаз, наприклад, твердої стінки, рідини і газу між поверхнею рідини і твердою стінкою утворюється так званий крайовий кут θ. Величина крайового кута залежить від природи дотичних середовищ (від поверхневих натягів на їхніх межах) і не залежить ні від форми посудини, ні від дії сили ваги. Якщо край рідини піднятий, її поверхня має увігнуту форму — крайовий кут гострий. У цьому разі рідина змочує тверду поверхню. Чим гірша змочувальна здатність рідини, тим більшим є крайовий кут. При θ>90° рідина вважається незмочувальною, при повному незмочуванні θ=180°. Краплі такої рідини немов би підгортаються, намагаючись зменшити площу контакту з твердою поверхнею. Капілярні явищаВід явища змочування залежить поведінка рідини в тонкій (капілярній) трубці, зануреній у неї. У разі змочування рідина в трубці піднімається над рівнем вільної поверхні, у протилежному випадку — опускається. Висоту капілярного підняття (опускання) рідини знаходять за формулою
де γ — питома вага рідини;
Перехід з рідкого у газоподібний стан і навпакиВипаровуванняВипаровування — це вид пароутворення в процесі поступового переходу речовини з рідкої в газоподібну фазу (пару) через вільну поверхню. При тепловому русі деякі молекули покидають рідину з її поверхні і переходять в пару. Разом з тим, частина молекул переходить назад з пари в рідину. Якщо з рідини виходить більше молекул, ніж приходить, то відбувається випаровування. Випаровування супроводжується зниженням температури, оскільки з рідини вилітають молекули з енергією, яка перевищує середню. Кількісно калориметрія випаровування характеризується питомою теплотою пароутворення — фізичною величиною, яка визначає кількість теплоти, що необхідна для випаровування 1 кг рідини за незмінної температури. Для води при 0 °C питома теплота пароутворення становить L = 2413 Дж/г. Тоді кількість теплоти, що поглинається при випаровування рідини масою m може бути визначена за формулою:
КонденсаціяКонденсація — зворотний до випаровування процес, перехід речовини з газоподібного стану в рідкий. При цьому в рідину переходить з пари більше молекул, ніж у пару з рідини. На відміну від випаровування, під час якого теплота поглинається, при конденсації теплота виділяється. ЇЇ кількість визначають за тією ж формулою, що і теплоту пароутворення. Питома теплота конденсації за значенням така сама, як і питома теплота пароутворення. КипінняКипіння — процес переходу рідини в пару, який характеризується, на відміну від випаровування, тим, що утворення пари відбувається не тільки на поверхні, але й в усій масі рідини. Кипіння можливе, якщо тиск насиченої пари рідини дорівнює внутрішньому тиску. Тому дана рідина, знаходячись під цим зовнішнім тиском, кипить за цілком визначеної температури. Зазвичай температуру кипіння приводять за атмосферного тиску. Наприклад, за атмосферного тиску вода кипить при 373 К або 100°С. КавітаціяКавітація — утворення всередині рідини порожнин (як і при кипінні), заповнених газом, парою або їх сумішшю (кавітаційних бульбашок), що приводить до порушення суцільності рідини. Кавітація виникає в результаті місцевого зниження тиску в рідині до певного критичного значення ркр (в реальній рідині значення ркр близьке до тиску насиченої пари цієї рідини при даній температурі), що може відбуватися або при збільшенні швидкості руху рідини (гідродинамічна кавітація), або при проходженні акустичної хвилі великої інтенсивності під час напівперіоду розрідження (акустична кавітація). Поширення звуку у рідинахОскільки рідини мають велику жорсткість лише за об'ємного стиснення і є податливими при зсувних деформаціях, швидкість звуку c у рідині буде визначатися величиною модуля всебічного стиску: де
У прісній воді звук поширюється приблизно із швидкістю 1497 м/с при 25 °C. Див. також
ПриміткиДжерела
Посилання
|
||||||||||||




















