Talium 81 Tlisotop dengan massa atom berkisar antara 176 hingga 216. Talium memiliki dua isotop stabil , 203 Tl dan 205 Tl. 204 Tl adalah radioisotop talium yang paling stabil dengan waktu paruh 3,78 tahun. 207 Tl, dengan waktu paruh 4,77 menit, memiliki waktu paruh terpanjang dari semua radioisotop talium alami. Semua isotop talium bersifat radioaktif atau stabil secara pengamatan , artinya mereka diprediksi bersifat radioaktif tetapi tidak ada peluruhan aktual yang teramati.
202 Tl (waktu paruh 12,23 hari) dapat dibuat dalam siklotron [ 2] 204 Tl (waktu paruh 3,78 tahun) dibuat dengan aktivasi neutron dari talium stabil dalam reaktor nuklir .[ 3]
Dalam keadaan terionisasi penuh, isotop 205 Tl dapat menjadi radioaktif, meluruh melalui peluruhan beta menjadi 205 Pb[ 4] 203 Tl tetap stabil.
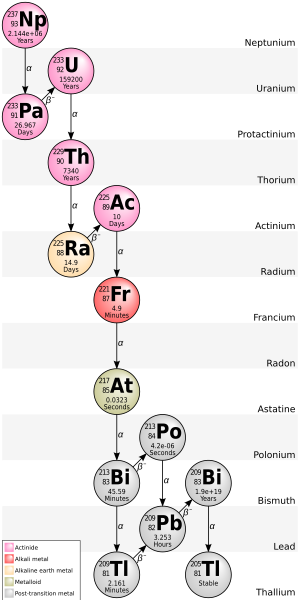
205 Tl merupakan produk peluruhan dari 209 Bipeluruhan alfa dengan waktu paruh yang sangat panjang, yaitu 2,01× 1019 tahun.[ 5] 205 Tl berada di ujung rantai peluruhan deret neptunium .
Rantai peluruhan deret neptunium , yang berakhir pada 205 Tl.
Daftar isotop
Nuklida[ 6] [ n 1]
Nama
Z N Massa isotop (Da ) [ 7] [ n 2] [ n 3] Waktu paruh [ n 4] Mode [ n 5] Isotop [ n 6] Spin danparitas [ n 7] [ n 4] Kelimpahan alami (fraksi mol)
Energi eksitasi[ n 4]
Proporsi normal
Rentang variasi
176 Tl
81
95
176,00059(21)#
5,2(+30−14) mdtk
(3−, 4−, 5−)
177 Tl
81
96
176,996427(27)
18(5) mdtk
p
176 Hg
(1/2+)
α (langka)
173 Au
177m Tl
807(18) keV
230(40) μs
p
176 Hg
(11/2−)
α
173 Au
178 Tl
81
97
177,99490(12)#
255(10) mdtk
α
174 Au
p (langka)
177 Hg
179 Tl
81
98
178,99109(5)
270(30) mdtk
α
175 Au
(1/2+)
p (langka)
178 Hg
179m Tl
860(30)# keV
1,60(16) mdtk
α
175 Au
(9/2−)
IT (langka)
179 Tl
180 Tl
81
99
179,98991(13)#
1,5(2) dtk
α (75%)
176 Au
β+ (25%)
180 Hg
EC, fisi (10−4 %)
100 Ru80 Kr[ 8]
181 Tl
81
100
180,986257(10)
3,2(3) dtk
α
177 Au
1/2+#
β+
181 Hg
181m Tl
857(29) keV
1,7(4) mdtk
α
177 Au
9/2−#
β+
181 Hg
182 Tl
81
101
181,98567(8)
2,0(3) dtk
β+ (96%)
182 Hg
2−#
α (4%)
178 Au
182m1 Tl
100(100)# keV
2,9(5) dtk
α
178 Au
(7+)
β+ (langka)
182 Hg
182m2 Tl
600(140)# keV
10−
183 Tl
81
102
182,982193(10)
6,9(7) dtk
β+ (98%)
183 Hg
1/2+#
α (2%)
179 Au
183m1 Tl
630(17) keV
53,3(3) mdtk
IT (99,99%)
183 Tl
9/2−#
α (0,01%)
179 Au
183m2 Tl
976,8(3) keV
1,48(10) μdtk
(13/2+)
184 Tl
81
103
183,98187(5)
9,7(6) dtk
β+
184 Hg
2−#
184m1 Tl
100(100)# keV
10# dtk
β+ (97,9%)
184 Hg
7+#
α (2,1%)
180 Au
184m2 Tl
500(140)# keV
47,1 mdtk
IT (99,911%)
(10−)
α (0,089%)
180 Au
185 Tl
81
104
184,97879(6)
19,5(5) dtk
α
181 Au
1/2+#
β+
185 Hg
185m Tl
452,8(20) keV
1,93(8) dtk
IT (99,99%)
185 Tl
9/2−#
α (0,01%)
181 Au
β+
185 Hg
186 Tl
81
105
185,97833(20)
40# dtk
β+
186 Hg
(2−)
α (0,006%)
182 Au
186m1 Tl
320(180) keV
27,5(10) dtk
β+
186 Hg
(7+)
186m2 Tl
690(180) keV
2,9(2) dtk
(10−)
187 Tl
81
106
186,975906(9)
~51 dtk
β+
187 Hg
(1/2+)
α (langka)
183 Au
187m Tl
335(3) keV
15,60(12) dtk
α
183 Au
(9/2−)
IT
187 Tl
β+
187 Hg
188 Tl
81
107
187,97601(4)
71(2) dtk
β+
188 Hg
(2−)
188m1 Tl
40(30) keV
71(1) dtk
β+
188 Hg
(7+)
188m2 Tl
310(30) keV
41(4) mdtk
(9−)
189 Tl
81
108
188,973588(12)
2,3(2) mnt
β+
189 Hg
(1/2+)
189m Tl
257,6(13) keV
1,4(1) mnt
β+ (96%)
189 Hg
(9/2−)
IT (4%)
189 Tl
190 Tl
81
109
189,97388(5)
2,6(3) mnt
β+
190 Hg
2(−)
190m1 Tl
130(90)# keV
3,7(3) mnt
β+
190 Hg
7(+#)
190m2 Tl
290(70)# keV
750(40) μdtk
(8−)
190m3 Tl
410(70)# keV
>1 μdtk
9−
191 Tl
81
110
190,971786(8)
20# mnt
β+
191 Hg
(1/2+)
191m Tl
297(7) keV
5,22(16) mnt
β+
191 Hg
9/2(−)
192 Tl
81
111
191,97223(3)
9,6(4) mnt
β+
192 Hg
(2−)
192m1 Tl
160(50) keV
10,8(2) mnt
β+
192 Hg
(7+)
192m2 Tl
407(54) keV
296(5) ndtk
(8−)
193 Tl
81
112
192,97067(12)
21,6(8) mnt
β+
193 Hg
1/2(+#)
193m Tl
369(4) keV
2,11(15) mnt
IT (75%)
193 Tl
9/2−
β+ (25%)
193 Hg
194 Tl
81
113
193,97120(15)
33,0(5) mnt
β+
194 Hg
2−
α (10−7 %)
190 Au
194m Tl
300(200)# keV
32,8(2) mnt
β+
194 Hg
(7+)
195 Tl
81
114
194,969774(15)
1,16(5) jam
β+
195 Hg
1/2+
195m Tl
482,63(17) keV
3,6(4) dtk
IT
195 Tl
9/2−
196 Tl
81
115
195,970481(13)
1,84(3) jam
β+
196 Hg2−
196m Tl
394,2(5) keV
1,41(2) jam
β+ (95,5%)
196 Hg(7+)
IT (4,5%)
196 Tl
197 Tl
81
116
196,969575(18)
2,84(4) jam
β+
197 Hg
1/2+
197m Tl
608,22(8) keV
540(10) mdtk
IT
197 Tl
9/2−
198 Tl
81
117
197,97048(9)
5,3(5) jam
β+
198 Hg2−
198m1 Tl
543,5(4) keV
1,87(3) jam
β+ (54%)
198 Hg7+
IT (46%)
198 Tl
198m2 Tl
687,2(5) keV
150(40) ndtk
(5+)
198m3 Tl
742,3(4) keV
32,1(10) mdtk
(10−)#
199 Tl
81
118
198,96988(3)
7,42(8) jam
β+
199 Hg1/2+
199m Tl
749,7(3) keV
28,4(2) mdtk
IT
199 Tl
9/2−
200 Tl
81
119
199,970963(6)
26,1(1) jam
β+
200 Hg2−
200m1 Tl
753,6(2) keV
34,3(10) mdtk
IT
200 Tl
7+
200m2 Tl
762,0(2) keV
0,33(5) μdtk
5+
201 Tl[ n 8]
81
120
200,970819(16)
72,912(17) jam
EC
201 Hg1/2+
201m Tl
919,50(9) keV
2,035(7) mdtk
IT
201 Tl
(9/2−)
202 Tl
81
121
201,972106(16)
12,23(2) hri
β+
202 Hg2−
202m Tl
950,19(10) keV
572(7) μdtk
7+
203 Tl
81
122
202,9723442(14)
Stabil Secara Pengamatan [ n 9] 1/2+
0,2952(1)
0,29494–0,29528
203m Tl
3400(300) keV
7,7(5) μdtk
(25/2+)
204 Tl
81
123
203,9738635(13)
3,78(2) thn
β− (97,1%)
204 Pb2−
EC (2,9%)
204 Hg
204m1 Tl
1104,0(4) keV
63(2) μdtk
(7)+
204m2 Tl
2500(500) keV
2,6(2) μdtk
(12−)
204m3 Tl
3500(500) keV
1,6(2) μdtk
(20+)
205 Tl[ n 10]
81
124
204,9744275(14)
Stabil Secara Pengamatan [ n 11] 1/2+
0,7048(1)
0,70472–0,70506
205m1 Tl
3290,63(17) keV
2,6(2) μdtk
25/2+
205m2 Tl
4835,6(15) keV
235(10) ndtk
(35/2–)
206 Tl
Radium E
81
125
205,9761103(15)
4,200(17) mnt
β−
206 Pb0−
Renik[ n 12]
206m Tl
2643,11(19) keV
3,74(3) mnt
IT
206 Tl
(12–)
207 Tl
Aktinium C
81
126
206,977419(6)
4,77(2) mnt
β−
207 Pb1/2+
Renik[ n 13]
207m Tl
1348,1(3) keV
1,33(11) dtk
IT (99,9%)
207 Tl
11/2–
β− (0,1%)
207 Pb
208 Tl
Torium C"
81
127
207,9820187(21)
3,053(4) mnt
β−
208 Pb5+
Renik[ n 14]
209 Tl
81
128
208,985359(8)
2,161(7) mnt
β−
209 Pb
1/2+
Renik[ n 15]
210 Tl
Radium C″
81
129
209,990074(12)
1,30(3) mnt
β− (99,991%)
210 Pb
(5+)#
Renik[ n 12]
β− , n (0,009%)
209 Pb
211 Tl
81
130
210,993480(50)
80(16) dtk
β− (97,8%)
211 Pb
1/2+
β− , n (2,2%)
210 Pb
212 Tl
81
131
211,998340(220)#
31(8) dtk
β− (98,2%)
212 Pb
(5+)
β− , n (1,8%)
211 Pb
213 Tl
81
132
213,001915(29)
24(4) dtk
β− (92,4%)
213 Pb
1/2+
β− , n (7,6%)
212 Pb
214 Tl
81
133
214,006940(210)#
11(2) dtk
β− (66%)
214 Pb
5+#
β− , n (34%)
213 Pb
215 Tl
81
134
215,010640(320)#
10(4) dtk
β− (95,4%)
215 Pb
1/2+#
β− , n (4,6%)
214 Pb
216 Tl
81
135
216,015800(320)#
6(3) dtk
β−
216 Pb
5+#
β− , n (<11,5%)
215 Pb
Header & footer tabel ini: view
^ m Tl – Isomer nuklir tereksitasi.^ ( ) – Ketidakpastian (1σ ) diberikan dalam bentuk ringkas dalam tanda kurung setelah digit terakhir yang sesuai.
^ # – Massa atom bertanda #: nilai dan ketidakpastian yang diperoleh bukan dari data eksperimen murni, tetapi setidaknya sebagian dari tren dari Permukaan Massa (trends from the Mass Surface , TMS).
^ a b c # – Nilai yang ditandai # tidak murni berasal dari data eksperimen, tetapi setidaknya sebagian dari tren nuklida tetangga (trends of neighboring nuclides , TNN).
^
Mode peluruhan:
^ Simbol tebal sebagai anak – Produk anak stabil.^ ( ) nilai spin – Menunjukkan spin dengan argumen penempatan yang lemah.
^ Isotop utama yang digunakan dalam skintigrafi
^ Diyakini mengalami peluruhan α menjadi 199 Au
^ Produk peluruhan akhir dari rantai peluruhan 4n+1 (deret neptunium )
^ Diyakini mengalami peluruhan α menjadi 201 Au
^ a b Produk peluruhan antara dari 238 U^ Produk peluruhan antara dari 235 U
^ Produk peluruhan antara dari 232 Th
^ Produk peluruhan antara dari 237 Np
Talium-201
Talium-201 (201 Tl) adalah sebuah radioisotop sintetis talium. Ia memiliki waktu paruh 73 jam dan meluruh dengan menangkap elektron , memancarkan sinar-X (~70–80 keV), dan foton 135 dan 167 keV dalam kelimpahan total 10%.[ 9] 201 Tl disintesis oleh aktivasi neutron talium stabil dalam reaktor nuklir ,[ 9] [ 10] 203 Tl(p, 3n)201 Pb di dalam siklotron , karena 201 Pb201 Tl sesudahnya.[ 11] radiofarmasi , karena memiliki karakteristik pencitraan yang baik tanpa dosis radiasi pasien yang berlebihan. Ia juga merupakan isotop paling populer yang digunakan untuk iskemia koroner inti talium.[ 12]
Referensi
^ Meija, J.; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)" . Pure Appl. Chem. 88 (3): 265–91. doi :10.1515/pac-2015-0305 . ^ "Thallium Research" . doe.gov . Departemen Energi AS . Diarsipkan dari versi asli tanggal 9 Desember 2006. Diakses tanggal 12 Juli 2022 . ^ Manual untuk radioisotop yang diproduksi oleh reaktor dari Badan Tenaga Atom Internasional ^ "Bound-state beta decay of highly ionized atoms" (PDF) . Diarsipkan dari versi asli (PDF) tanggal 29 Oktober 2013. Diakses tanggal 12 Juli 2022 . ^ Marcillac, P.; Coron, N.; Dambier, G.; et al. (2003). "Experimental detection of α-particles from the radioactive decay of natural bismuth". Nature . 422 (6934): 876–878. Bibcode :2003Natur.422..876D . doi :10.1038/nature01541 . PMID 12712201 . ^ Waktu paruh, mode peluruhan, spin nuklir, dan komposisi isotop bersumber dari:Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF) . Chinese Physics C . 41 (3): 030001. Bibcode :2017ChPhC..41c0001A . doi :10.1088/1674-1137/41/3/030001 .
^ Wang, M.; Audi, G.; Kondev, F. G.; Huang, W. J.; Naimi, S.; Xu, X. (2017). "The AME2016 atomic mass evaluation (II). Tables, graphs, and references" (PDF) . Chinese Physics C . 41 (3): 030003–1—030003–442. doi :10.1088/1674-1137/41/3/030003 . ^ Reich, E. S. (2010). "Mercury serves up a nuclear surprise: a new type of fission" . Scientific American . Diakses tanggal 12 Juli 2022 . ^ a b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties" , Nuclear Physics A , 729 : 3–128, Bibcode :2003NuPhA.729....3A , doi :10.1016/j.nuclphysa.2003.11.001 ^ "Manual for reactor produced radioisotopes" (PDF) . Badan Tenaga Atom Internasional . 2003. Diarsipkan dari versi asli (PDF) tanggal 21 Mei 2011. Diakses tanggal 12 Juli 2022 . ^ Cyclotron Produced Radionuclides: Principles and Practice (PDF) . Badan Tenaga Atom Internasional . 2008. ISBN 9789201002082 . Diakses tanggal 12 Juli 2022 . ^ Maddahi, Jamshid; Berman, Daniel (2001). "Detection, Evaluation, and Risk Stratification of Coronary Artery Disease by Thallium-201 Myocardial Perfusion Scintigraphy 155" . Cardiac SPECT imaging (edisi ke-2nd). Lippincott Williams & Wilkins. hlm. 155–178. ISBN 978-0-7817-2007-6 . Diarsipkan dari versi asli tanggal 22 Februari 2017. Diakses tanggal 12 Juli 2022 .
Massa isotop dari:
Komposisi isotop dan massa atom standar dari:
"News & Notices: Standard Atomic Weights Revised" . International Union of Pure and Applied Chemistry . 19 Oktober 2005. Data waktu paruh, spin, dan isomer dipilih dari sumber-sumber berikut.
Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties" , Nuclear Physics A , 729 : 3–128, Bibcode :2003NuPhA.729....3A , doi :10.1016/j.nuclphysa.2003.11.001 National Nuclear Data Center. "NuDat 2.x database" . Laboratorium Nasional Brookhaven . Holden, Norman E. (2004). "11. Table of the Isotopes". Dalam Lide, David R. CRC Handbook of Chemistry and Physics Boca Raton, Florida : CRC Press . ISBN 978-0-8493-0485-9 .