|
Kalium ferisianida
Kalium ferisianida adalah sebuah senyawa anorganik dengan rumus kimia K3[Fe(CN)6] yang terdiri dari ion kalium dan ferisianida, [Fe(CN)6]3−. SintesisKalium ferisianida dihasilkan dengan mengalirkan gas klorin dalam larutan kalium ferosianida.
PenggunaanSenyawa ini biasanya digunakan dalam cetak biru dan sianotip dalam bidang fotografi. Selain itu, kalium ferisianida juga digunakan untuk menguatkan besi dan merupakan sebuah pengoksidasi lemah dalam kimia organik. Kalium ferisianida juga digunakan dalam larutan indikator feroksil dengan fenolftalein untuk menangkap ion Fe2+ untuk pengesanan pengoksidasian besi yang membawa kepada perkaratan. Larutan tersebut berubah warna menjadi biru (biru Prusia) dengan kehadiran ion tersebut. Biru PrusiaPigmen biru Prusia yang digunakan dalam cetak biru dihasilkan dengan reaksi kalium ferisianida dengan garam ion ferus (Fe2+) juga dengan garam dari ion feri (Fe3+).[2] Referensi
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
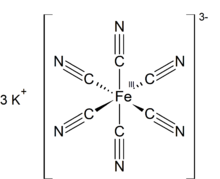

![{\displaystyle {\ce {2 K4[Fe(CN)6] + Cl2 -> 2 K3[Fe(CN)6] + 2 KCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4bdbff7964c1e6b75ddbc7a9ec7880756bbe5b88)