|
อินโดล
อินโดล (อังกฤษ: Indole) เป็นสารประกอบอินทรีย์ประเภทอะโรมาติกเฮเทอโรไซคลิก มันเป็นโครงสร้าง 2 วงแหวน (bicyclic structure) ส่วนที่เป็น 6 เหลี่ยมเรียกเบนซีนเชื่อมกับวงแหวน 5 เหลี่ยมที่มีอะตอมไนโตรเจน 1 อะตอม เชื่อมต่อกับคาร์บอน 4 อะตอมซึ่งเรียกว่า วงแหวน ไพร์โรล (pyrrole) การเชื่อมต่อไนโตรเจนกับวงแหวนอะโรมาติก มีความหมายว่าอินโดลจะประพฤติตัวไม่เป็นด่าง และมันก็ไม่เป็นเอมีนธรรมดา อินโดลเป็นของแข็งที่อุณหภูมิห้องมีกลิ่นคล้ายอุจจาระ แต่ที่ความเข้มข้นต่ำๆ มันจะมีกลิ่นดอกไม้ โครงสร้าง อินโดล สามารถพบได้ในสารประกอบอินทรีย์มากมายเช่น กรดอะมิโน ทริปโตแฟน (tryptophan) ในอัลคะลอยด์ หรือ ในปิกเมนต์ อินโดล (indole) เป็นคำที่ได้จาก อินดิโก (indigo) เป็นสีน้ำเงินที่ได้จากพืชชนิดหนึ่ง โมเลกุลของอินดิโก ประกอบด้วยโครงสร้างอินโดล 2 หน่วยมาเชื่อมกัน
ประวัติ (History) การศึกษาคุณสมบัติทางเคมีของอินโดลเริ่มที่การศึกษาสี อินดิโก (indigo) เริ่มจากการเปลี่ยน ไอสาติน (isatin)ออกซินโดล (oxindole) และในปี 1866 อดอล์ฟ วอน ไบเออร์ (Adolf von Baeyer) ได้รีดิว ออกซินโดล ไปเป็น อินโดล โดยใช้ สังกะสีเป็นตัวเร่งปฏิกิริยา การสังเคราะห์อินโดลอินโดลเป็นส่วนประกอบหลักของโคล-ทาร์ มีวิธีสังเคราะห์ดังนี้ การสังเคราะห์อินโดลแบบ ไลม์กรูเบอร์-แบตโช (Leimgruber-Batcho) การสังเคราะห์อินโดลแบบ ไลม์กรูเบอร์-แบตโช เป็นวิธีที่มีประสิทธิภาพที่สุดในการสังเคราะห์อินโดล และส่วนประกอบของมัน และถูกจดสิทธิบัตรในปี 1976วิธีนี้ให้ผลผลิตสูงที่สุดและนิยมมากที่สุดใน เภสัชอุตสาหกรรม การสังเคราะห์อินโดลแบบฟิสเซอร์ (Fischer) การสังเคราะห์อินโดลแบบฟิสเซอร์เป็นวิธีที่นิยมและเก่าแก่มากที่สุดซึ่งคิดค้นและพัฒนาในปี 1883 โดย อีมิล ฟิสเซอร์ (Emil Fischer) การสังเคราะห์อินโดลแบบอื่นๆ
ปฏิกิริยาเคมีของอินโดลElectrophilic substitution กรามีน (Gramine) สามารถเตรียมได้จากปฏิกิริยาแมนนิช (Mannich reaction)ของอินโดลกับ ไดเมตทิลามีน (dimethylamine) และ ฟอร์มาดิไฮด์ (formaldehyde)  Nitrogen-H acidity and organometallic indole anion complexes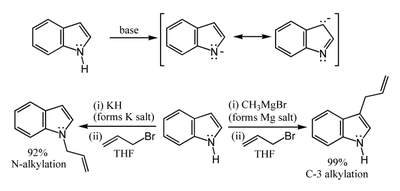 Carbon acidity and C-2 lithiation Oxidation of indole Cycloadditions of indole การใช้ประโยชน์มะลิ (jasmine)ในธรรมชาติและ น้ำมันหอมระเหย ที่ใช้ในอุตสาหกรรมน้ำหอม มีอินโดลประมาณ 2.5 % กลิ่นมะลิที่สกัดจากธรรมชาติจะมีราคากิโลกรัมละ $10,000 แต่ถ้า สังเคราะจากอินโดลจะมีราคาเพียง $10/kg ดูเพิ่ม
อ้างอิง
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
