|
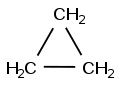
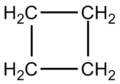
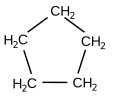
CicloalcaniI cicloalcani (o nafteni[1]) sono composti organici monociclici saturi (cioè che non contengono legami doppi o tripli tra atomi di carbonio) costituiti solamente da atomi di carbonio e di idrogeno (e per questo appartenenti alla più ampia classe degli idrocarburi).[2] Appartengono inoltre alla classe dei composti aliciclici (che comprende inoltre i cicloalcheni e i cicloalchini). Esempi di cicloalcani sono il ciclobutano e il cicloesano. Simili agli alcani, si differenziano da questi ultimi in quanto nella loro struttura gli atomi di carbonio sono uniti a formare un anello chiuso. Quando il numero di atomi di carbonio nell'anello è 3 (ciclopropano) o 4 (ciclobutano), gli atomi di carbonio sono forzati a formare legami con angoli molto piccoli, 60° e 88° rispettivamente, ben inferiori al valore di 109,5° tipico della struttura tetraedrica. Questa forzatura produce una tensione (detta tensione d'anello) che rende la molecola meno stabile. Un esempio estremo di molecola in tensione è quello del cubano. Nomenclatura IUPAC
Le formule utilizzate in questo esempio sono formule di struttura semplificate. Ogni vertice rappresenta un atomo di carbonio e gli atomi di idrogeno direttamente legati ad essi non sono evidenziati - con l'eccezione degli atomi dei gruppi legati ai cicli, voluta in questo caso dall'autore per evidenziare i criteri di assegnazione dei nomi. cicloesano metilciclopentano 1,2-dietilcicloesano Isomeria nei cicloalcaniNei cicloalcani, data la loro particolare struttura tridimensionale non lineare, manca la possibilità di avere rotazione libera di legami come ad esempio negli n-alcani. Nonostante questa maggior rigidità, i cicloalcani possono manifestare fenomeni di isomeria e questa è data dalla posizione dei loro sostituenti rispetto al piano orizzontale. I sostituenti possono infatti presentarsi sulla stessa faccia e saranno quindi in cis (a) oppure presentarsi su facce opposte ed essere quindi in trans (b). A differenza degli isomeri di struttura i sostituenti sono legati nello stesso ordine ma hanno disposizione tridimensionale differente. Composti con queste proprietà sono definiti stereoisomeri. Fonti industrialiLe reazioni condotte su scala maggiore sono l'addizione di idrogeno al benzene e ad altri composti aromatici sostituiti per convertirli nei corrispondenti cicloesani. Data la stabilità degli anelli aromatici, la reazione richiede un catalizzatore e condizioni di lavoro piuttosto drastiche. Generalmente il catalizzatore è nichel, l'idrogeno viene mantenuto a pressioni non inferiori alle 15 atmosfere e la temperatura di reazione a non meno di 150 °C. Preparazioni per sintesiI ciclopropani si preparano per
R-CH=CH-R' + CH2N2 → R-CH---CH-R'
\ /
CH2
CH2---CH2
Cl-CH2-CH2-CH2-Cl + Zn → \ /
CH2
I cicloalcani superiori ed i sistemi policiclici possono venire preparati ricorrendo alle reazioni elettrocicliche; tra esse la più comune è la reazione di Diels-Alder tra un diene ed un alchene sostituito con gruppi elettron-attrattori (detto dienofilo). La reazione produce un cicloalchene che viene successivamente idrogenato (vedi alcheni) a cicloalcano. Reazioni tipicheI cicloalcani hanno una reattività pressoché identica a quella degli alcani. Come questi sono infiammabili e subiscono facilmente reazioni di sostituzione radicalica catalizzate dalla luce o dal calore. Per via della tensione d'anello, il ciclopropano reagisce con idrogeno attraverso apertura dell'anello, trasformandosi in propano: CH2---CH2 \ / + H2 → CH3-CH2-CH3 CH2 o con acidi alogenidrici attraverso apertura dell'anello, trasformandosi nei corrispondenti propani alogenati: CH2---CH2 \ / + HX → CH3-CH2-CH2-X CH2 NoteVoci correlateAltri progetti
Collegamenti esterni
|